Hygienemerkblätter (HMB) der UMR
Hepatitis B/C/D
Meldepflicht
Verdacht, Nachweis, Erkrankung, Tod namentlich zu melden an:
Gesundheitsamt
Abteilung Infektionsschutz
Paulstraße 22
18055 Rostock
0381 381 9552
- Pflichtformular laut Infektionsschutzgesetz § 6 (1)
- Formulare sind hier bzw. im SAP abrufbar
- Meldepflichtig ist der feststellende Arzt
Darüber hinaus ist der direkte oder indirekte Nachweis durch den Leiter des diagnostizierenden Labor namentlich zu melden:
- für HBV und HDV im Fall des Hinweises auf eine akute Infektion;
- für HCV für alle Nachweise, sofern nicht bekannt ist, dass eine chronische Infektion vorliegt (§ 7 (1) IfSG)
Erreger
Hepatitis B-Virus
Hepatitis C-Virus
Hepatitis D-Virus (nur in Verbindung mit Hepatitis B-Virus-Infektion)
Infektiöses Material
Körperflüssigkeiten,
- insbesondere Blut;
- Sperma,
- Vaginalsekret
Übertragungsweg
- Stich- und Schnittverletzungen,
- sonstige ggf. auch kleine Verletzungen,
- Schleimhautkontakt,
- Aerosole bei Verletzung des Patienten im Respirationstrakt (z. B. zahnärztliche Behandlung!)
Inkubationszeit
HBV
40-200 Tage
(im Durchschnitt 60-90 Tage)
HCV
2-24 Wochen
(im Durchschnitt 6-9 Wochen)
Dauer der Infektiosität
HBV
Bei ca. 80 % der Betroffenen wegen spontaner Ausheilung
- < ½ Jahr
Bei den restlichen 20 % ohne eine spezifische Behandlung sowie bei der überwiegenden Mehrzahl von HCV-Infizierten ohne eine spezifische Behandlung:
- langfristig
(d. h. im Bereich von Jahren, wenn nicht lebenslang)
Für HDV-Infizierte bestimmt die aktive HBV-Infektion die Infektiosität.
Für HBV- und HCV-Infizierte gilt:
Die Infektiosität sinkt unter einer spezifischen Therapie innerhalb weniger Wochen in der Regel unter die Gefahrengrenze.
Gegen HBV geimpfte Mitarbeiter und Kontaktpatienten sind in der Regel gegen die HBV-Infektion geschützt (ggf. Impftiter rasch bestimmen lassen).
Diagnostik (zum Erstnachweis bzw. Verlauf)
Serum auf Antikörper und Antigene,
Ggf. EDTA-Blut für die PCR in die Virologie
Viruslast mittels PCR (Virologie) zur Bestimmung der Infektiosität
Hygienemaßnahmen/Schutzmaßnahmen
Isolierung/Entisolierung
In der Regel nicht erforderlich
Ausnahme: Blutender Patient, unkontrollierbar aggressiver bzw. verwirrter Patient;
Eine eigene Toilette/Toilettenstuhl ist in der Regel nicht notwendig.
Ausnahme: Unbehandelter, schwer lenkbarer HBV-Patient mit unkontrollierbaren Blutungen (z. B. bei Fissuren, Hämorrhiden, Menses).
Kontaktpatienten
Von Indexpatienten mit geringer HBV-Viruslast bzw. unter laufender anti-HBV-Therapie sowie von HCV-Patienten geht in der Regel keine Gefahr für Mitpatienten aus.
Ferner sind gegen HBV geimpfte Kontaktpatienten nicht gefährdet.
Besucher
Standardhygiene ist ausreichend.
Es gelten daher keine weiteren Einschränkungen für Besucher, Studierende und Mitarbeiter anderer Bereiche.
Ambulanter Bereich/Aufwachraum
Standardhygiene ist ausreichend.
Händedesinfektion
Händedesinfektion gemäß Basishygieneordnung.
Alle im Hause verfügbaren Händedesinfektionsmittel sind geeignet.
Einwirkzeit beachten!
Einmalhandschuhe
Erforderlich bei Kontakt mit erregerhaltigem Material, Körperflüssigkeiten oder Ausscheidungen.
Nach dem Ablegen hygienische Händedesinfektion!
Schutzkittel
Erforderlich, wenn mit Verspritzen von kontaminiertem Material gerechnet werden muss.
Mund-Nasen-Schutz/Schutzbrille
Erforderlich, wenn mit Aerosolbildung oder Verspritzen von Blut, Körperflüssigkeiten oder Ausscheidungen zu rechnen ist (z. B. Intubation, Absaugung, etc.).
Wäscheentsorgung
Entsorgung im fest verschlossenen Wäschesack.
Geschirr
Geschirrspülautomat, Betriebstemperatur > 60°C
Sofern vorhanden, chemisch-thermische Desinfektion mit Gewerbegeschirrspüler
Pflege-/Behandlungs- und Untersuchungsgeräte und-Hilfsmittel (Medizinprodukte)
Nach Gebrauch desinfizierend reinigen bzw. Aufbereitung nach Herstellerangaben bzw. verwerfen.
Abfallentsorgung
Normale Entsorgung (‘‘Krankenhausspezifische Abfälle‘‘- AS180104/180101/Abfallgruppe B);
Fäzes und Urin in die Kanalisation
Flächendesinfektion
Desinfektion nach Kontamination, bei Entlassung bzw. routinemäßig laut Basishygieneordnung
(siehe BHO/Desinfektion).
Desinfektionsmittel laut Desinfektionsplan
Patiententransfer
Beim Transport sind keine Besonderheiten zu beachten.
Standardhygiene ist ausreichend.
Besonderheiten im OP
Neben der allgemeinen Standardhygiene im OP oder der Funktionsabteilung ist das Tragen von doppelten Handschuhen sowie Gesichtsschutz (Augenschutz) sinnvoll.
Besonderheiten für das Personal
Nicht-immunes Personal
(mit Patientenkontakt, Labor- und Entsorgungspersonal sowie Reinigungspersonal) muss sich einer Impfung unterziehen (ArbSchG!), ansonsten ist eine Beschäftigung mit Expositionsrisiko nicht möglich.
Simultanimmunisierung nur bei HBV-Exposition:
ist bei nicht-immunem Personal postexpositionell umgehend zu veranlassen.
Bei Rückfragen Information durch den Betriebsärztlichen Dienst!
Schwangere Mitarbeiterinnen
Kontakt mit dem Patienten ist unter strikter Einhaltung der Standardhygieneregeln erlaubt.
Invasive Maßnahmen dürfen nicht durchgeführt werden.
Stand: August 2020
Hepatitis B/C/D
- HBV.pdf[25 KB]
Weiterführende Informationen
Einsenderhinweise
(Auszug Einsenderhinweise IMIKRO)
Hepatitis B- und D-Viren
Hepatitis B- und D-Viren
Verfahren | Antigennachweis Antikörpernachweis Nachweis von Nukleinsäure |
Indikation |
|
Material | Serologie/PCR
|
Methode |
|
Lauris- | Serologie
PCR
|
Weiterführende Informationen | Hygienemerkblatt der UMR Nadelstichverletzung Folgende Parameter gehören zur Routinediagnostik: Indexpatient
Verletzter(betroffener Mitarbeiter)
Das Hepatitis-D-Virus wird nur bei Menschen mit aktiver HBV-Infektion nachgewiesen. Eine Abklärung des HDV-Trägerstatus wird, zumindest einmal initial, bei allen Patienten mit einer nachgewiesenen Hepatitis B empfohlen. Eine HBV-Genotypisierung bei Erstnachweisen, eine genotypische Resistenztestung sowie die Bestimmung der Hepatitis-D-RNA erfolgen nach Versand in ein Fremdlabor. |
Aktualisiert: Januar 2025
Hepatitis B- und D-Viren
Hepatitis C-Virus
Hepatitis C-Virus
Verfahren | Antikörpernachweis Nachweis von RNA |
Indikation |
|
Material | Serologie/PCR
|
Methode |
|
Lauris- | Serologie
PCR
|
Weiterführende Informationen | Hygienemerkblatt der UMR Nadelstichverletzung Folgende Parameter gehören zur Routinediagnostik: Indexpatient
Verletzter (betroffener Mitarbeiter)
Für die Beurteilung einer Infektiosität ist die molekularbiologische Bestimmung der Viruslast erforderlich. Die HCV-Genotypisierung erfolgt nach Versand in ein Fremdlabor. |
Aktualisiert: Januar 2025
Hepatitis C-Virus
Zeitliches Bearbeitungsschema
H
(Auszug zeitliches Bearbeitungsschema IMIKRO)
Erreger | Nachweisart | Geeignete Materialien | Mo | Di | Mi | Do | Fr | Sa | So |
|---|---|---|---|---|---|---|---|---|---|
Haemophilus influenzae | PCR | Li. | x | x | x | x | x | x | x |
Haemophilus influenzae | Kultur | siehe "mögliche Materialien" | x | x | x | x | x | x1 | x1 |
Hantavirus | AK | Ser. | x | x | x | x | x | x1 | x1 |
Helicobacter pylori | AG | Stu. | x | x | x | ||||
Helicobacter pylori | Kultur | Magenbioptat | x | x | x | x | x | x1 | x1 |
Helicobacter pylori | PCR | Gew., Stu. | auf Anforderung | ||||||
Hepatitis A-Virus | AK | Ser. | x | x | x | x | x | ||
Hepatitis A-Virus | PCR | EDTA-Bl., Stu. | x | x | x | x | x | ||
Hepatitis B-Virus
| AG | Ser. | x | x | x | x | x | ||
Hepatitis B-Virus
| AK | Ser. | x | x | x | x | x | ||
Hepatitis B-Virus
| PCR | Ser., EDTA-Bl. | x | ||||||
Hepatitis C-Virus | AK | Ser. | x | x | x | x | x | ||
Hepatitis C-Virus | PCR | Ser., EDTA-Bl. | x | ||||||
Hepatitis E-Virus | AK | Ser. | x | x | |||||
Hepatitis E-Virus | PCR | EDTA-Bl., Stu. | x | x | x | x | x | ||
Humanes Herpesvirus 1 (Herpes Simplex Virus 1, HSV1) | AK | Ser. | x | x | x | ||||
Humanes Herpesvirus 1 (Herpes Simplex Virus 1, HSV1) | AK-Index | Ser.-Li. Paar | x | ||||||
Humanes Herpesvirus 1 (Herpes Simplex Virus 1, HSV1) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr. | x |
| x |
| x | x1 | |
Humanes Herpesvirus 2 (Herpes Simplex Virus 2, HSV2) | AK | Ser. | x | x | x | ||||
Humanes Herpesvirus 2 (Herpes Simplex Virus 2, HSV2) | AK-Index | Ser.-Li. Paar | x | ||||||
Humanes Herpesvirus 2 (Herpes Simplex Virus 2, HSV2) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr. | x |
| x |
| x | x1 | |
Humanes Herpesvirus 3 (Varizella Zoster Virus, VZV) | AK | Ser. | x | x | x | ||||
Humanes Herpesvirus 3 (Varizella Zoster Virus, VZV) | AK-Index | Ser.-Li. Paar | x | ||||||
Humanes Herpesvirus 3 (Varizella Zoster Virus, VZV) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr. | x |
| x |
| x | x1 | |
Humanes Herpesvirus 4 (Epstein-Barr-Virus, EBV) | AK | Ser. | x | x | x | ||||
Humanes Herpesvirus 4 (Epstein-Barr-Virus, EBV) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr. | x | x | x | x | x | x1 | |
Humanes Herpesvirus 5 (Cytomegalievirus, CMV) | AK | Ser. | x | x | x | ||||
Humanes Herpesvirus 5 (Cytomegalievirus, CMV) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr., Ur. | x | x | x | x | x | x1 | |
Humanes Herpesvirus 6 (HHV6 A/B) | PCR | EDTA-Bl., AWM, Li., Gew., Abstr. | x |
| x |
| x | x1 | |
Humanes Immundefizienz-Virus (HIV) | AK | Ser. | x | x | x | x | x | x3 | x3 |
Humanes Immundefizienz-Virus (HIV) | PCR | EDTA-Bl. | x | ||||||
Humanes Metapneumovirus (hMPV) | PCR | AWM | x | x | x | x | x | ||
Humanes Parechovirus | PCR | Li. | x | x | x | x | x | x | x |
Humanes Polyomavirus 1 (BK-Virus) | PCR | EDTA-Bl., Li., Ur. | x | x | |||||
Humanes Polyomavirus 2 (JC-Virus) | PCR | EDTA-Bl., Li., Ur. | x | x | |||||
Aktualisiert: April 2026
Legende Wochentage
Symbol | Erklärung |
|---|---|
x | Bearbeitung der Materialien bei Probeneingang bis 18:00 Uhr |
x1 | Bearbeitung der Materialien bei Probeneingang bis 10:30 Uhr |
x2 | sofortige Bearbeitung nur bei Augenabstrichen (Keratokonjunktivitis epidemica), sonst am Folgetag |
x3 | sofortige Bearbeitung der HIV-Serologie im Rahmen von Nadelstichverletzungen (NSV) |
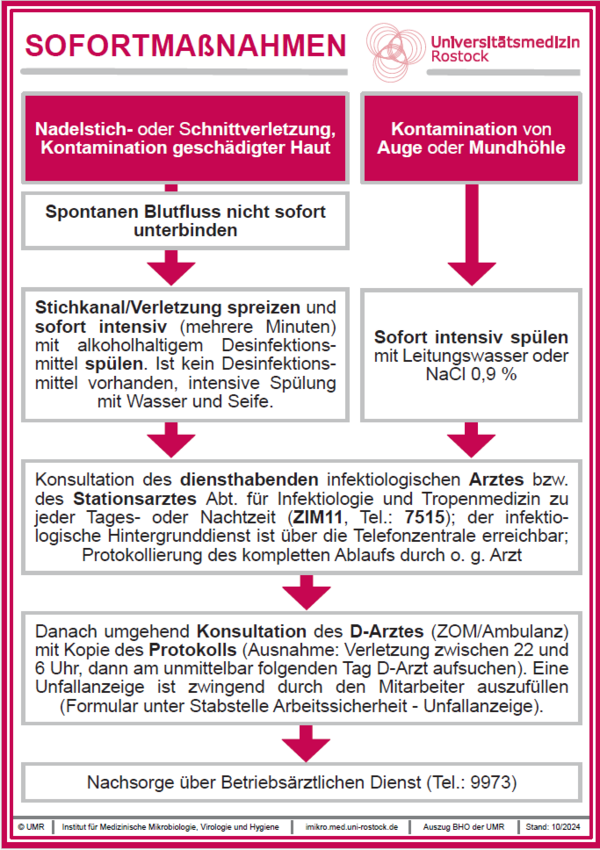
Sofortmaßnahmen Nadelstichverletzung
(Auszug Basishygieneordung der UMR)
Schema Sofortmaßnahmen
Inhaltsverzeichnis
Hygienemerkblätter der UMR
Inhalt E
- EAEC
- EHEC
- EIEC
- Encephalopathie
- Entamoeba histolytica
- Enteritiden (Bakt.)
- Enteritiden (Inv. Bakt.)
- Enteritiden (Viral)
- Entero-aggregative E. coli
- Enterobius vermicularis
- Entero-hämorrhagische E. coli
- Entero-invasive E. coli
- Entero-pathogene E. coli
- Entero-pathogene Yersinien
- Entero-toxische E. coli
- Enterokokken
- Enteroviren
- EPEC
- ETEC